一、教学目标
1、知识与技能
(1)理解电解质、非电解质的概念。
(2)理解电离的概念,学会写电离方程式。
2、过程与方法
(1)通过实验探究和问题探究引导学生自主学习,从电离的角度得出酸、碱、盐的定义。
(2)运用多媒体辅助教学,在激发学生的求知欲望、提高学生的学习兴趣的同时,也培养了学生善于思考、勇于发现问题和解决问题的能力。
3、情感态度与价值观
(1)通过探究培养学生实验操作能力和描述实验现象、归纳实验结论的能力。
(2)通过学生动手实验,体验化学的奥妙,激发学生学习兴趣。
二、教学重点、难点
电解质、非电解质的概念。
三、教学方法
实验探究法,自主学习法,归纳总结法,讲授法。
四、课前准备
1.学生的学习准备:课前预习学案。
2.教师的教学准备:多媒体课件制作,课前预习学案,课内探究学案。准备实验用品及仪器。
五、课时安排:1课时
六、教学过程
(一)预习检查、总结疑惑
检查落实学生的预习情况并了解了学生的疑惑,使教学具有了针对性。
(二)教学过程
【实验探究】
利用下图装置进行实验,请你认真观察、记录现象并对现象做出解释。
1、在烧杯中放入氯化钠固体
2、取出碳棒并擦净,插入盛有纯水的烧杯中
3、将氯化钠固体逐勺加入纯水中
实验步骤、现象、解释现象、形成规律:
1、在烧杯中放入氯化钠固体,灯泡不亮,离子不能自由移动,某些物质溶于水离解成自由移动的离子后能导电,且离子浓度越大,导电能力越强。
2、取出碳棒并擦净,插入盛有纯水的烧杯中灯泡不亮,自由移动的离子浓度太小。
3、将氯化钠固体逐勺加入纯水中,灯泡逐渐变亮,氯化钠溶于水后能离解成自由移动的离子。
离子反应
一、酸、碱、盐在水溶液中的电离
1、电解质的定义:
思考:酸、碱、盐在水溶液中为什么能导电?它们与金属导电有什么不同?
2、电解质溶液导电原因
3、电离
1)下列物质:铜,硫酸,氯化钠固体,氯化钾溶液,氢氧化钾固体,碳酸钙,二氧化碳,蔗糖,硫酸溶液进行分类,哪些是电解质?
2)氯气的水溶液能导电,氯气是不是电解质?为什么?
3)二氧化碳的水溶液能导电,二氧化碳是不是电解质?为什么?
(2)电解质的导电条件:只有在水溶液或熔融状态。即电解质本身不一定能导电;如氯化钠固体;反之能导电的也不一定就是电解质,如铜、氯化钾溶液
(3)电解质导电必须是化合物本身能电离出自由移动的离子而导电。
(4)正确理解“和”与“或”
【引导学生归纳】
【动画演示】氯化钠在水中的溶解和电离。
【总结】电离的概念:物质溶于水后或受热熔化时,离解成能够自由移动的离子的过程。
【过渡】怎样表示氯化钠的电离呢?
【引入】电离的表示方法--------电离方程式
重点分析氯化钠的电离方程式:NaCl=Na++Cl-,强调原子守恒和电荷守恒。
【探究练习】
请分别书写下列各组物质的电离方程式,并从电离的角度认识酸、碱和盐。
1、硫酸、硝酸
2、氢氧化钾、氢氧化钡
3、硫酸铜、氯化钡
【学生板书】
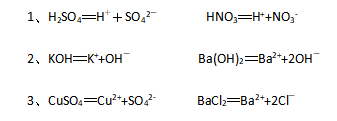
【教师分析】酸的定义:电离时生成的阳离子全部是H+的化合物
【思考与交流1】请参考酸的定义,尝试从电离的角度概括出碱和盐的本质。
【学生归纳】碱:电离时生成的阴离子全部是OH-的化合物。
盐:电离时生成金属离子(或NH4+)和酸根离子的化合物。
【思考和交流2】
1、已知NaHSO4电离方程式为:NaHSO4=Na++H++SO42-,请问NaHSO4属于酸类还是盐类?
2、还有哪些物质溶于水能电离出离子而导电呢?
【学生讨论】酸、碱、大多数盐
【引入】电解质的概念:在水溶液里或熔融状态下能够导电的化合物叫做电解质。
【问题探究】下列物质属于电解质的是:
A、铝线B、加碘食盐C、氯化钠D、氯气E、蔗糖水溶液 F、酒精G、盐酸H、二氧化碳
【学生讨论】理解电解质时应该注意哪些问题
【学生归纳】
(1)电解质为化合物,这是判断前提。单质、混合物(如:盐酸溶液)不是电解质。
(2)电解质的导电是有条件的,即电解质必须在水溶液里或熔融状态下才能导电。而且是本身电离而导电的化合物。
(3)能导电的物质并不一定是电解质,如铜、铝、石墨等不是电解质。
(4)H2SO4、NaOH、NaCl等酸、碱、盐类物质是电解质,Na2O、Al2O3等部分金属氧化物也是电解质
【设疑】酒精在水溶液中和熔融状态都不能导电,它属于哪类物质呢?
【引入】非电解质的概念:在水溶液里和熔融状态下均不能导电的化合物叫做非电解质。
【问题探究】下列物质属于非电解质的是:
A、铝线B、加碘食盐C、氯化钠D、氯气E、蔗糖水溶液
F、酒精G、盐酸H、二氧化碳
【学生归纳】单质和混合物既不是电解质也不是非电解质。
七、板书设计
离子反应
一、酸、碱、盐在水溶液中的电离
1、电离
物质溶于水后或受热熔化时,离解成能够自由移动的离子的过程。
2、电离的表示方法-------离子方程式
如:NaCl=Na++Cl-(原子守恒、电荷守恒)
3、电解质
在水溶液里或熔融状态下能够导电的化合物叫做电解质。
4、非电解质
在水溶液里和熔融状态下均不能导电的化合物叫做非电解质。
八、教学反思
本课的设计采用了课前下发预习学案,学生预习本节内容,找出自己迷惑的地方。课堂上师生主要解决重点、难点、疑点、考点、探究点以及学生学习过程中易忘、易混点等,最后进行当堂检测,课后进行延伸拓展,以达到提高课堂效率的目的。










